Генетический код сложнее его триплетной модели
Гаряев П.П.
Генетический код сложнее его триплетной модели
Сейчас, вот парадокс, мы видим, что положение в генетике, как основе биологического знания, оставляет ощущение искусно нарисованного, красивого и опасного миража. Это после провала знаменитой программы «Геном человека», когда обывателю, он же налогоплательщик, стали внушать — наконец-де «прочтена вся» генетическая информация человеческих хромосом. Послышались восклицания о прорывных успехах трансгенной инженерии, клонировании животных и вот-вот человека. Но какова реальность? Итог программы «Геном человека» вывел нас на «зияющие высоты» официальной генетики. Теперь мы знаем последовательность 3 миллиардов нуклеотидов в ДНК наших хромосомах. И что? Так и осталось непонятным главное, стратегическое, мировоззренческое — каким образом мы, люди, и вообще все Живое, закодировано в собственных хромосомах. Вот характерное высказывание на этот счет, сделанное Эмманюэлем Тевеноном в журнале LABEL в статье «Науки о живых организмах: конец «всесильной» генетике?»: «Несмотря на значительные затраченные средства, терапевтические итоги развития генетики оставляют желать лучшего. До такой степени, что исследователи начинают пересматривать саму концепцию дисциплины, главенствующей в биологической науке вот уже на протяжении пятидесяти лет». Был постулирован «момент истины» — все заложено в генах. И это была парадигма на десятилетия. После открытия двойной спирали ДНК возникла теоретическая схема: структура ДНК имеет участки, гены, которые, кодируя белки, а также РНК, определяют внешность живого организма и управляет его поведением. Словно всемогущий демиург геном представлялся творцом организма, который объясняет в этом организме все. Такое представление о «всесильной» генетике усилилось с появлением международного проекта расшифровки генома человека, в котором приняли участие США, Великобритания, Франция, Германия, Япония и Китай. Считалось a priori, что все записано в триплетном коде белковых генов. И поэтому достаточно будет локализовать «неправильный» ген, чтобы затем нейтрализовать его нежелательную функцию. Средства массовой информации ежедневно рассказывали о продвижении исследований, сообщая, что они приведут к созданию новых лекарств. Но и через десять лет после секвенирования генома вируса СПИДа прививка против него так и не создана. Генетическая терапия, породив небывалые надежды, привела пока к чрезвычайно малым результатам. Из сотен клинических опытов, проведенных во многих странах мира, лишь один привел к реальному исцелению: французским врачам под руководством Марины Кавацана-Кальво и Алена Фишера (Inserm U 429, клиника им. Неккера в Париже) удалось вылечить десять детей, страдавших тяжелым недостатком иммунной системы. Однако и этот успех оказался недолгим: в октябре 2002 г. у одного из детей обнаружен побочный эффект в виде лейкемии, что повело за собой остановку клинических испытаний. Одновременно США также остановили часть программ по развитию генной терапии. В наши дни генетики возлагают надежды на то, что расшифровка генома человека позволит определить тысячи генов, характеризующих каждое человеческое существо. Примерно десять – двенадцать тысяч уже были определены, но конкретные функции установлены пока только у 5000.
Приведем один пример: в 2001г. с огромной помпой была объявлена расшифровка генома мушки дрозофилы (Drosophila melanogaster), и в то же время в Европе насчитывалось только два специалиста, способных сравнить и идентифицировать 3000 разных вида дрозофилы. Несоответствие очевидно. Чтобы выйти из эпистемологического тупика, в который зашла генетика, два французских ученых, специалисты по молекулярной биологии Жан-Жак Купек и Пьер Саниго, предлагают применить к их дисциплине теорию Дарвина, порвав таким образом с современным детерминизмом. В книге «Ни Бога, ни гена», опубликованной недавно, они объясняют, что сообщество клеток организма определяется не генетической программой, а конкуренцией, которая происходит между различными составляющими живого организма в целях получения внешних ресурсов, без которых он не может жить. Молекулы возникают произвольным образом и принцип «естественного» отбора поощряет жизненно способные сочетания. Как и большинство высших организмов (растения, животные и др.), выживают и развиваются те молекулы и клетки, которые лучше других способны найти питание. Эта теория, возможно, объясняет тот факт, что генетики не могут до сих пор разработать вакцину против ВИЧ. Ее невозможно создать, поскольку она должна делать невозможное — быстро реагировать на миллиарды изменений в минуту у миллиардов индивидуумов. Это столь же бессмысленно, как и изучение, атом за атомом, строения автомобиля в целях усиления дорожной безопасности. Так что же в итоге сей грандиозной программы? «Прочитали» геном у шести людей — по одному мужскому и женскому каждой из трех разных рас плюс геном Крэга Ветера, ведущего ‘программиста’ Генома человека. Нашлись между ними кое-какие отличия, консенсусную последовательность составить не удается. Основная масса генов практически идентична от кишечной палочки до человека. Словом, «гора родила мышь». Разочарование. В среде ученых-генетиков начался разброд и шатание. Базовый элемент генетики – ген, удивительное дело, постепенно выходит за рамки ее понимания. Раздаются даже голоса научных паникеров, призывающих отказаться от изучения генома и заменить его изучением всех известных белков, создать направление под названием протеомика. Это вместо геномики. Рассуждают при этом примерно так: коль скоро мы не можем понять, как на самом деле работает генетический аппарат и молекула ДНК, давайте отойдем в сторону и займемся детальным изучением всех белков. Тогда уж точно поймем, каким образом строится организм, и по каким законам. Только это – не более чем повтор той же ошибки, что и с геномом, поскольку белки являются полиаминокислотными репликами ДНК. В перспективе снова видится кризис, но уже не геномный, а протеомный. И снова с огромной затратой денег и научной энергии впустую. Отмывка денег «по научному»? Известный биолог Брюс Липтон еще более категоричен в своей статье «Программа Геном Человека – космическая шутка, заставившая ученых кататься по полу от смеха» http://www.money-health-relationships.com/human-genome-project.html . Он предвидит переворот в биологии как следствие отказа от концепции генов как управляющих биосистемой структур. Этот переворот он понимает как аналог такового в физике, шагнувшей от Ньютоновских представлений в квантовые. Наступает эра квантовой (волновой) генетики?Истоки ошибок
Почему же генетика, а вместе с ней и биология, не могут выйти из этого заколдованного круга непонимания реальных механизмов хромосомного кодирования? Как сейчас понимают ген? Что-то изменилось в этом плане со времени открытия двойной спирали ДНК? Для этого обратимся к «официальной» молекулярной биологии и генетике, взяв фундаментальный и относительно новый учебник, одним из создателей которого является соавтор этой самой модели двойной спирали ДНК, нобелевский лауреат Джеймс Уотсон: Б.Альбертс, Д.Брей, Дж.Льюис, М.Рэфф, Дж.Уотсон. Молекулярная биология клетки. Т.3. М. Изд. «Мир» (1994). Заметим, что к моменту настоящего анализа (2008г.) принципиальных сдвигов в понимании генетического кода официальной генетикой не произошло и, соответственно, в учебниках тоже. Ни одно из базовых положений в этой области знания официальной биологией не пересмотрено, хотя обнаружено многое, грозящее разрушить эту базу. Что же такого грозного для официальной генетики обнаружено уже давно и в недавних исследованиях? Анализируем её классические положения напрямую, по страницам названного классического учебника для ВУЗов:
Стр. 99-101: Излагается теория позиционной информации Вольперта [Wolpert, 1971], теория, которая вот уже более 30 лет лежит в основе объяснений, каким образом осуществляется молекулярное (генетическое) руководство строительством 4-х мерной (пространственно-временной) структуры многоклеточного организма. Читаем: «Во многих развивающихся системах небольшие участки ткани способны приобретать какие-либо особые свойства, превращающие их в источник сигнала, который распространяется через прилежащие участки ткани, и может контролировать их поведение. В частности, сигналом могут служить диффундирующие молекулы, секретируемые сигнализирующим участком. Возникает концентрационный градиент. Чем дальше ткань-источник, тем меньше сигнал. Гипотетическое вещество, … концентрация которого прочитывается клетками и позволяет последним определить расстояние относительно неких ориентиров или «маяков», называется морфогеном. Сигнализирующий участок способен с помощью морфогена контролировать формирование пространственной организации больших полей прилежащих тканей. Градиенты морфогена представляют собой простое и эффективное средство обеспечения клеток позиционной информацией».
«И хотя известно множество примеров сигнализирующих участков, … на практике в настоящее время мы имеем дело всего лишь с несколькими случаями непосредственной химической идентификации морфогена. Как правило, известно лишь, что изменения местоположения предполагаемого сигнализирующего участка после пересадки или иным способом, происходит изменение структуры прилежащих участков ткани. Наблюдения такого рода не позволяют выяснить, насколько изменения структуры отдельных клеток определяются прямым ответом на действие морфогена и каков вклад от взаимодействия реагирующих клеток. Вероятно, в большинстве случаев исходный градиент морфогена вызывает импульс, обеспечивающий формирование пространственной организации широкого спектра действия, а локальные межклеточные взаимодействия участвуют в проработке деталей… морфоген может действовать в поле клеток, каждая из которых реагирует независимо… в отсутствии морфогена может срабатывать «эффект «запоминания»».
Итак, в соответствии со сказанным, развитие эмбриона определяют некие гипотетические морфогены, идентификация которых чрезвычайно редкое событие и природа которых не обязательно родственна или тождественна генетическим структурам, то есть ДНК или РНК. И совершенно таинственное утверждение, что морфоген может действовать в «поле клеток». Что это за «поле», не уточняется. Фигурируют никак не трактуемые термины (понятия?), например, «запись» позиционной информации на уровне «клеточной памяти» с образованием некоего «позиционного значения». Что есть память клетки, опять-таки, не объясняется. Но то, что она должна быть «хорошей» подчеркивается поскольку «морфогены действуют на расстояниях не более 1мм», то есть примерно 100 или менее клеточных диаметров. Именно это вызывает необходимость авторам вводить никак не трактуемое понятие «клеточной памяти». Авторы пишут: «…различие между головой и хвостом в эмбрионе должно закладываться еще тогда, когда длина соответствующих участков не превышает 1 мм …. К тому времени, когда длина животного достигнет сантиметра или метра, события, в результате которых возникли эти различия, будут уже «древней историей»; и для того, чтобы данные различия сохранялись, клетки должны обладать хорошей памятью». Запомним эти ключевые слова и словосочетания-понятия, введенные в этом фрагменте, но никак не объясненные: клеточная память, клеточное поле, запись информации. А также важный для будущих размышлений факт, что морфогенетическая информация действует в эмбрионе на расстояние не более 1 мм.
Cтр. 102. «Конечное состояние клетки возникает как результат определенной последовательности решений».
Еще один термин, походя введенный авторами – «клеточные решения». Ни слова о том, кто и каким образом «решает».
Стр. 105. «Весьма вероятно, что природным морфогеном является … ретиноевая кислота. …Удалось идентифицировать рецептор ретиноевой кислоты. Им оказался белок, гомологичный рецепторам стероидных и тиреоидных гормонов; он связывается с определенными последовательностями ДНК и регулирует транскрипцию определенных генов».
Это иллюстрация сказанного ранее – морфогены не обязательно выступают в форме нуклеиновых кислот, то есть это, собственно, не гены. В основном это белки, иногда такие простые соединения как ретиноевая кислота.Далее авторы делают откровенное признание, упорно игнорируемое «официальной» генетикой: «Молекулярные механизмы, лежащие в основе этого важного способа контроля роста пока не известны».
Стр. 109. Далее еще более удивительно: «Вся классическая генетика основана на предположении о том, что строение любого организма контролируется его генами. Роль ДНК в обеспечении наследственности известна уже более 100 лет, однако механизмы генетического контроля, которые отвечают за образование нормальной структуры тела взрослых животных, до сих пор остаются неразгаданными. В последние годы этот пробел в наших знаниях начал заполняться. Опыты на дрозофиле привели к открытию класса контролирующих развитие генов, специфическая функция которых состоит в формировании пространственной организации тела. Это гомеозисные селекторные гены. Продукты этих генов служат молекулярными адресами, в первом приближении обеспечивающими клетки позиционными значениями. Гомеозисные мутации… нарушают нормальное обеспечение информацией всех клеток данного участка: клетки дезинформируются в отношении своего местоположения и из них формируются структуры, которые в норме располагаются в иных участках тела».
Без каких-либо объяснений введено еще одно понятие — «молекулярные адреса» гомеозисных селекторных генов. Звучит красиво, но непонятно. Каким образом продукты селекторых генов, то есть белки, играют роль адресов для перемещающихся эмбриональных клеток, которые при этом еще и по непонятным командам превращаются в другие — мышечные, костные, нервные и т.д.? Более того, напоминаем, что действие морфогенов распространяется в эмбрионе не более, чем на 1-2 мм. Как могут работать молекулярные адреса морфогенов в эмбрионе, если их действие столь ограничено в пространстве? Ответа нет. Имеются только декларативные и противоречивые утверждения, что вновь подтверждает отсутствие понимания главного в работе генома, каким образом кодируется структура организма.
Cтр. 117. «Несколько генов из каждой группы генов сегментации было клонировано и соответствующие зонды использованы для локализации транскриптов в нормальных эмбрионах по методу гибридизации in situ». Так были получены транскрипты гена bicoid и других генов, участвующих в организации структуры развивающихся эмбрионов. Далее читаем — «Транскрипты гена bicoid являются источником позиционного сигнала: транскрипты локализуются на одном из концов яйца дрозофилы, хотя эффекты мутации гена распространяются на большую часть эмбриона».
Вот еще одно кричащее противоречие между экспериментами и «официальной» теорией. Поясняем. РНК-транскрипты генов морфогенеза и, соответственно, их продукты-белки синтезируются локально в определенных ограниченных участках эмбриона, а их, белков, морфогенетическое действие распространяется за пределы мест биосинтеза этих белков, на большую часть эмбрионов. Это означает, что мы видим явное несоответствие теории позиционной информации об ‘градиент-ограниченном’ действии морфогенов. Противореча сами себе, авторы, тем не менее, дают великолепный иллюстративный экспериментальный материал о локализации морфогенов в одном месте эмбрионов и проявлении их действия на расстояниях, запредельно удаленных от места начального появления и дифффузии морфогенов. Иными словами, налицо, странным образом игнорируемое, дальнодействие селекторных белков морфогенеза. В этом обнаруживается одна из реализаций фундаментального генетического (эмбрионального) явления – нелокальности действия белков морфогенеза. Скажем проще. Белок (или белки), управляющие пространственной (и временной) организацией эмбриона, изначально и локально находятся в одном месте пространства зародыша, а действие их проявляется совершенно в другом, отдаленном участке эмбриона, куда они не могут диффундировать с достаточной скоростью, чтобы напрямую оказать регуляторное действие. Иными словами, их функция реализуется нелокально. Проявляется пространственное дальнодействие белковых факторов эмбриогенеза. Это фундаментальный факт. Но он просто-напросто не замечается основной частью «официальной» эмбриологии/генетики и в очередной раз заводит в логический тупик. Почему так? Ответ прост – объяснение этого феномена, равно как и многих других «аномальных» особенностей генома многоклеточных, неизбежно приводит генетику, и биологию в целом, к существенно иным толкованиям работы хромосом.
Продолжим критический анализ. Аналогичный эффект нелокальности был зафиксирован также и для гена Kruppel. Авторы пишут: «Можно предположить по аналогии с bicoid, что белок Kruppel в роли диффундирующего морфогена распространяется из участка транскрипции Kruppel, хотя наблюдаемое распространение белка не столь обширно, как требуется в соответствии с этой гипотезой». Имеется в виду гипотеза (теория) градиентов морфогенов Вольперта. Простая диффузия белков морфогенеза – слишком медленный процесс, чтобы объяснить непонятное: белок здесь, а действие его в другом, отдаленном месте, куда он не проник. Это важное признание. И снова выступает упорно не замечаемый фактор дистантности, быстрой, не диффузионной, дальнодействующей эмбриональной информации, природа которой непонятна авторам. Никак не берется в расчет, что выход белков, как крупных молекулярных структур, за пределы клетки является отнюдь не простым актом диффузии (как в случае газов или растворов), а сложным, энергозатратным и длительным процессом экзоцитоза. Вышедший из клетки белок, чтобы достичь места своего локального (вещественного) действия, должен вновь быть захвачен другой клеткой, являющейся преградой для путешествия белка к месту своего действия. Этот захват белка (эндоцитоз) – также сложный и длительный процесс. Таким образом, прохождение морфогенов (по крайней мере, белковой природы) через клеточные слои к месту действия это сложный, длительный и многоактный процесс, исключающий то, что мы видим на самом деле — реальные быстрые, дальние дистантные переносы программирующих активностей белков-морфогенов. Почему бы авторам ни задаться простым вопросом – а не смысловые ли, не текстовые ли конструкции белков-морфогенов являются целью дистантной (волновой) передачи на большие межклеточные, межтканевые расстояния? Это тем более логично, если учесть, что никаких собственных, непосредственно организующих морфогенез, актов у гомеозисных белков не обнаружено. Они входят в цитоплазму клеток и выполняют непонятную по механизмам эмбрионально-регуляторную функцию. Затем они связываются с определенными участками хромосомной ДНК, чтобы индуцировать синтез следующего белка-морфогена. Последний, сделав очередной, с виду бесцельный, вояж по цитоплазме, вновь активирует следующий селекторный ген, продуцирующий следующий белок-морфоген, и т.д. Видна картина каскадной иерархической (фрактальной) регуляции активности генов морфогенеза. Картина красивая, но непонятная в главном – как же всё-таки осуществляется, собственно, сама морфогенез-программирующая функция гомеозисных белков и почему они действуют дистантно? Полная беспомощность эмбриологов по этому ключевому вопросу прекрасно продемонстрирована, например, в обзоре известного исследователя Л.Корчкина — http://www.neurogene.ru/2003a4.htm. Все соображения здесь, по сути, сводятся к простой констатации активности тех или иных генов морфогенеза, синтезирующих те или иные белковые продукты. Генеральные мотивации процесса морфогенеза, их природа остаются за пределами понимания. Это выглядит примерно так, как если бы мы пытались понять живописное полотно, анализируя, сколько красок использовано для создания картины и каков их химический состав. Итог такого анализа будет жалким – Джоконда предстанет перед нами как 200 граммов разных маслянистых веществ, определенным образом размазанных по текстилю. Не аллегория ли на программу «Геном человека»?
Смотрим дальше.
Стр. 118-119. «…иерархия позиционных сигналов должна соответствовать иерархии регуляторных взаимодействий между генами, управляющими формированием пространственной организации. Это положение можно проверить при изучении влияния мутации одного гена на экспрессию другого. Оказалось, что гены, участвующие в процессе формирования пространственной организации вдоль переднезадней оси эмбриона, формируют иерархическую пирамиду в пяти основных ярусах, причем продукты генов каждого яруса регулируют экспрессию генов нижележащих ярусов. На вершине этой пирамиды находятся гены полярности яйца (так называемые «мастер гены» или «гены-господа»
Г.П.), за ними gap-гены, затем гены pair-rule, затем гены полярности сегментов и, наконец, гомеозисные селекторные гены. Можно получить мутантные эмбрионы, лишенные нормальных продуктов гена Kruppel, и определить методом гибридизации in situ экспрессию нормального гена ftz, используя клонированный зонд, комплементарный последнему. Характерные полосы радиоавтографов Kruppel не образуются именно в тех участках бластомеры, которые затронуты мутацией Kruppel. Следовательно, продукт гена Kruppel прямо или косвенно регулирует экспрессию гена ftz. Вместе с тем, у мутантов ftz распределение нормального продукта Kruppel не нарушено: продукт ftz не регулирует экспрессию гена Kruppel. Иногда гены взаимно ингибируют друг друга с образованием четких границ экспрессии их продуктов».
В этом цитируемом фрагменте видна еще одна в высшей степени характерная деталь, свойственная всем работам по регуляции генов морфогенеза. В них говорится о чем угодно, кроме главного. А главное заключается в стратегических мотивах и механизмах эмбриогенетических функций продуктов генов морфогенеза, то есть соответствующих белков. В чем программирующие эмбрион действия этих генов? Какова конкретная функция этих белков? Нет ответа. Вместо этого приводят сложную и, надо заметить, точную иерархию того, как гены последовательно включают-выключают друг друга посредством собственных белковых продуктов. Невольно складывается впечатление, что «включательно-выключательные» операции белков морфогенеза — их единственные регуляторно-метаболические назначения в цитоплазме эмбриональных клеток. Единственные ли? Явно не единственные, поскольку результирующая их активности – эмбриогенез, который, естественно, не может сводиться к включениям-выключениям генов и их сетевым связям. Это типичная ситуация т.н. «черного ящика» — на входе Ген (белок), а на выходе Функция, Признак. Мы хотим заглянуть внутрь черного ящика и поэтому задаем вопрос: так в чем же основная работа генов и их продуктов, белков, по организации эмбриогенеза? Можно и нужно сформулировать вопрос даже предельно широко: каково происхождение и эволюция кодирующих функций хромосом? Ответа нет, и не будет, пока не пересмотрим существующие и догматизированные позиции генетического кодирования. Положение даже усложнилось. Hox-гены, считавшиеся ключевыми в процессах онтогенеза, сами регулируемы микро РНК-транскриптами. Они кодируются участками ДНК, расположенными между Hox-генами и считавшимися бессмысленными. Некоторые из таких микро РНК усиливают или ослабляют экспрессию самих Hox-генов, некоторые косвенно влияют на работу других транскрипционных факторов. Кроме того, микро РНК могут регулировать как соседние, так и отдаленные Hox-гены [Lemons, McGinnis, 2006]. Итак, что или кто главный регулятор, программист эмбриогенеза? Ниже регуляторных микро РНК только низкомолекулярные метаболиты и ионы. Causa finalis неясна. Возвращаемся к энтелехии Аристотеля-Дриша?
Причины, заставляющие изменять и дополнять понимание генетических функций, очевидны и намечены уже недвусмысленными сентенциями уважаемых авторов анализируемого учебника. Однако основная часть биологов неохотно расстаётся с иллюзиями, даже если они озвучены, как здесь, признанным авторитетом, нобелиатом, – Уотсоном и соавторами. Кроме того, в науке, как и на любом рынке, мощно действует система торговых брэндов. Таковым, к сожалению, стал и триплетный генетический код. Многолетний анализ обширной мировой литературы по генетике и молекулярной биологии показывает, что ареал ученых, публично пытающихся переосмыслить, казалось бы, устоявшиеся каноны генетики, весьма ограничен. Кроме наших исследований, это работы Дзян-Каньдженя [Jiang Kanzhen, 1981, 1991, 1994-1996, 1998, 1999, 2000] и научной школы акад. В.П.Казначеева [Казначеев В.П. и др, 1973; Казначеев В.П., Михайлова Л.П., 1985]. В какой-то мере этому направлению соответствуют работы Мосолова [Мосолов А.Н., 1980], Ричарда Миллера [Miller, 2003] и Поппа [http://www.biophotonik.de/], а также исследования Бурлакова [Бурлакова, 1999; Бурлаков и др., 2000]. О Ричарде Алане Миллере надо сказать особо. Он и Вебб первые в 1973 году высказали идею о том, что генетический аппарат может функционировать на принципах голографии [Miller, Webb, 1973], за что на долгие годы был предан «генетической анафеме».
Каковы же первоистоки заблуждений в генетике, этой, вроде бы, благополучной и успешной области биологического знания? Представляется, что начало кризиса, как ни парадоксально, положено триумфом открытия двойной спирали ДНК и ее функций Уотсоном и Криком в 1953г. с последующими усилиями по разработке принципов кодирования белков. Это был действительно мощный прорыв в понимании функций хромосом. Но увидели только половину правды, а то и меньше. Эйфория этих открытий с последующим их «забрендиванием» на долгие десятилетия перекрыла путь к пониманию дополнительных, главных генетических функций ДНК. Они лежат в иных знаковых ареалах генома – волновых, квантово нелокальных, текстовых [Гаряев, Тертышный, Товмаш, 2007; Гаряев, Кокая, Мухина и др., 2007; Гаряев, Кокая, Леонова-Гаряева, 2007; Гаряев, 2008 (подг. к печати)]. Однако эта часть генетической идеологии и экспериментов – предмет особой аналитической статьи.Ульф Лагерквист первый указал на неполноту триплетной модели генетического кода
Так в чем же конкретно таилось недопонимание принципов генетического кодирования? Оно в излишней жесткости модели триплетного кода как чисто физико-химической системы работы рибосомной машины и в неоправданном приписывании триплетной модели кода всех генетических атрибутов. Это ложное представление, основанное исключительно на принципе комплементарности взаимодействия оснований информационной РНК (иРНК) и транспортной РНК (тРНК), когда аденин «узнает» урацил, а гуанин «узнает» цитозин в процессе кодон-антикодонового «считывания» рибосомой информации с иРНК. Белковый код понимается как некий универсальный и единственный вектор всей генетики и всей эмбриологии. Каноническая таблица генетического кода стала своего рода фетишем, священной коровой или, если угодно, женой цезаря, которая вне подозрений. Только однажды была опубликована работа, осторожно бросившая лёгкую тень сомнения на модель триплетного кода, но не привлекшая к себе никакого внимания. Уотсон-Криковский нобелевский триумф и все последующие успехи в исследовании белоксинтезирующего аппарата, казалось, вели к сияющим высотам полного понимания работы человеческого и прочих геномов.
Упомянутая работа с первыми сомнениями была опубликована в 1978 году. В ней завуалированно демонстрировалась противоречивость и неполнота триплетной модели генетического кода, но исследование это было явно недооценено научной общественностью. Вернее, просто проигнорировано. Это была статья Ульфа Лагерквиста и называлась она ««Два из трех». Альтернативный метод кодонового чтения» [Lagerkvist, 1978]. Рассмотрим ее внимательно.
Лагерквист пишет: «Генетический код является универсальным, высоко вырожденным, трехбуквенным кодом, в котором первые две позиции кодона читаются антикодоном строго в соответствии с правилами классического спаривания оснований. Третья позиция в кодоне, однако, создает принципиальные проблемы для обоснования самой парадигмы шифрования белков. Так существует расхождение между большим числом кодонов в вырожденном коде и ограниченным числом антикодонов, способных к чтению этих кодонов. Этот провал попытался заполнить в 1966г. Ф.Крик своей изощренной (ingenious) гипотезой [Crick, 1966]. В этой классической работе Крик предположил, точнее, констатировал, что нуклеотид в 1’- позиции антикодона занимает «воблирующую» (от англ. wobble – качание) позицию и может фактически взаимодействовать с 3’-позицией кодона без соблюдения правил классического, термодинамически выгодного, спаривания оснований[1]. Далее Лагерквист приводит примеры таких «неправильных» спариваний оснований, подтвержденных экспериментально на бесклеточных рибосомальных системах, а также примеры таких спариваний, которые запрещены даже Вобл гипотезой. Основываясь на этих работах, он задает естественный и сакраментальный вопрос: приложимо ли это аномальное поведение (при спаривании 3’-1’ нуклеотидов в кодон-антикодоновых парах) к синтезу белков in vivo? Очевидный ответ, что правила Вобл гипотезы должны работать во всех ситуациях, в которых участвуют Вобл позиции, а это автоматически ведет к ошибкам в синтезе белка. Например, для аминокислот Phe/Leu кодоновая группа (UUU, UUC,UUA и UUG) на антикодоне с ‘G’ в Вобл позиции не может узнать кодоны UUA и UUG, что ведет к ошибке и введению в синтезируемый белок Phe вместо Leu.
Для большей иллюстративности мы приводим таблицу генетического кода, представленную Лагерквистом и перегруппированную им по кодоновым семействам с ориентировкой на первые два рабочих нуклеотида:
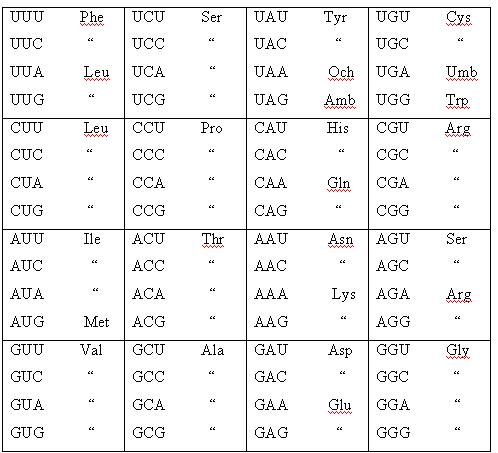
Лагерквист разместил коды аминокислот триплетами нуклеотидов (кодонами) в форме составных групп из 4-х кодонов, которые имеют общие первые два нуклеотида, а третий (3’) взаимодействует по водородным связям с первым (1’) нуклеотидом антикодона и при этом он, первый, «воблирует», т.е. de facto случаен. Если быть точнее, то 3-й кодоновый нуклеотид не участвует в кодировке аминокислот, хотя и детерминирован хромосомной ДНК. Если абстрагироваться от реальности, 3-й может быть любым из четырех возможных нуклеотидов. Поэтому в каждой четверке триплетов 3-й нуклеотид кодона чередуется в условной одинаковой монотонной последовательности U,C,A,G. Когда все четыре кодона распределены по сходным аминокислотам, тогда эти четверки образуют кодоновые семейства. Но в таком распределении по сходным аминокислотам имеется нюанс: одни и те же аминокислоты попадают в разные семейства. Например, Leu (лейцин) попадает в два семейства (если семейства определять не по аминокислотам, а по первым двум нуклеотидам в кодоне) – в семейства UU и СU. Аминокислота Ser (серин) попадает в семейства UC и AG. Аминокислота Arg (аргинин) попадает в семейства CG и AG. Однако есть и достоинство такой классификации семейств кодонов: отчетливо видна противоречивость модели триплетного кодирования аминокислот в первичной структуре белка. Это кодирование в действительности дублетное, но никак не триплетное. Лагерквист пишет: «.. в условиях белкового синтеза in vitro кодон может быть «прочитан» тРНК путем узнавания только первых двух его нуклеотидов, а нуклеотид в третьей позиции кодона игнорируется». Он констатировал, в общем-то, очевидный для всех принцип кодонового прочтения как «два из трех», но до Лагеквиста никто не акцентировал внимания на этом немаловажном факте. И напрасно. Если дело обстоит именно так, то белок синтезирующая система имеет источник потенциальных ошибок при совместном использовании рибосомой и тРНК правила «два из трех» для чтения кодонов иРНК антикодонами тРНК. Из Табл.1. видно, что одна и та же аминокислота может кодироваться четверками кодоновых семейств. Например, четверка CU-семейства кодирует лейцин. Четверка GU-семейства кодирует валин, UC – серин, CC – пролин, AC – триптофан, GC – аланин, CG –аргинин, GG – глицин. Это лежащий на поверхности, и сразу замеченный, факт вырожденности, т.е. информационной избыточности кода. Если взять взаймы понятия и термины лингвистики для белкового кода, что давно, повсеместно и с легкостью принято, то вырожденность кода можно понимать как синонимию. Это также единогласно принято. Иначе говоря, один и тот же объект, например, аминокислота, имеет несколько шифров — кодонов. Синонимия не таит в себе никаких опасностей для точности биосинтеза белков. Наоборот, такая избыточность хороша, поскольку повышает надежность работы трансляционной рибосомной «машины».
Однако на Табл.1 видно и другое, фундаментальное, генолингвистическое явление, как бы не замечаемое. Или игнорируемое. Это явление обнаруживается в том, что в некоторых кодоновых семействах четверки кодонов, точнее, их значащие одинаковые двойки нуклеотидов шифруют не одну, а две различные аминокислоты, а также стоп-кодоны. Так, дублетное UU-семейство кодирует фенилаланин и лейцин, AU – изолейцин и метионин, UA – тирозин, Och и Amb стоп-кодоны, CA – гистидин и глицин, AA – аспарагин и лизин, GA – аспарагиновую и глутаминовую, UG – цистеин, Umb и Trp стоп-кодоны, AG – серин и аргинин. Продолжая лингвистические аналогии, назовем это явление ОМОНИМИЕЙ первых двух кодирующих нуклеотидов в некоторых кодоновых семействах.
В отличие от синонимии, омонимия потенциально опасна, что и отметил Лагерквист, хотя и не ввел термин-понятие ‘омонимия’ в применении к белковому коду. Такая ситуация, вроде бы, действительно должна вести к неоднозначности кодирования аминокислот и стоп-сигналов: один и тот же кодоновый дублет, в пределах некоторых выделенных Лагерквистом семейств, кодирует две разных аминокислоты или является дважды стоповым. Эти особые кодоновые семейства можно свести в Табл.2. Для более четкого восприятия третьи кодоновые нуклеотиды (3’), не участвующие в кодировании аминокислот, обозначены маленькой буквой в нижнем индексе.
Табл.2.
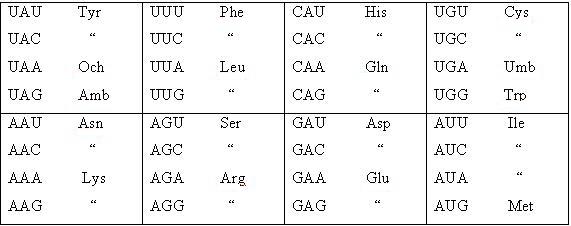
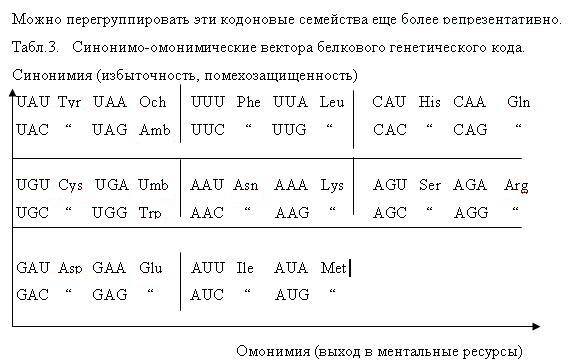
Такая завершающая перегруппировка дублетных кодоновых семейств и неоднозначно шифруемых ими аминокислот (а также функций стоп-кодонов) позволяет отчетливо увидеть омонимию триплетного кода в целом. Из восьми кодоновых семейств, систематизированных по значащим дублетам, пять омонимичны. Это выражает тот непреложный и не замечаемый (игнорируемый) факт наличия второго, омонимичного, многозначного измерения триплетного кода. Код знаково синонимо-омонимичен. И это фундаментальное явление.
Принципиально важно понять: если синонимия кода – это благо (избыток информации), то омонимия – потенциальное зло (неопределенность, неоднозначность информации). Но мнимое зло, поскольку белок синтезирующий аппарат легко обходит эту трудность, чем речь пойдет ниже. Если же автоматически следовать таблице (модели) генетического кода, тогда зло становится не мнимым, но реальным. И тогда очевидно, что омонимический вектор кода ведет к ошибкам в синтезе белков, поскольку рибосомный белоксинтезирующий аппарат, каждый раз встречаясь с тем или иным омонимичным дублетом и руководствуясь правилом чтения «два из трех», должен выбрать одну и только одну аминокислоту из двух различных, но кодируемых неоднозначно тождественными дублетами-омонимами. А также принять решение (в случае UA-семейства) – остановить синтез пептидной цепи (выбрать стоп кодон) или включить в ее состав тирозин. Если выбор неправилен (а как выбрать, таблица кода нам не сообщает), это приведет к ошибкам в синтезе белков. Потенциально опасная омонимия, ведущая к неправильному «прочтению» кодона антикодоном, следует из случайности (не знаковости) бытия 1’-нуклеотида антикодона, связывающегося с 3’- кодоном в омонимичных кодонах. Такую случайность многие оспаривают, апеллируя к Криковским Вобл-правилам кодон-антикодонового спаривания. Поставим точки над i.
Ф.Крик пытался снять странности неканонического поведения пары ‘3-й —1-й’ с помощью т.н. «Вобл гипотезы» [Crick, 1966]. Она вводит понятие неоднозначного соответствия кодонов аминокислотам в ген-кодируемых белках и говорит о возможности не канонического и случайного спаривания первого нуклеотида антикодона транспортной РНК (тРНК) с третьим нуклеотидом кодона информационной РНК (иРНК) при ее трансляции в белок[1]. Проще говоря, при биосинтезе белков иногда реализуется возможность нестрогого соответствия кодон-антикодоновых нуклеотидов в этом
[1] Обозначения: 1-й, 2-й и 3-й нуклеотиды в кодонах и антикодонах – это для упрощения понимания. Тогда 1-й, 2-й и 3-й нуклеотиды в кодонах спариваются с 3-м, 2-м и 1-м нуклеотидами в антикодонах с учетом антипараллельности триплетов. Если быть точным с точки зрения химии полинуклеотидов, то 3-й «воблирующий» нуклеотид в кодоне – это т.н. 3’- нуклеотид, а комплементарный ему 1-й нуклеотид антикодона – это 5’- нуклеотид.
положении. Это значит, что образуются неканонические пары оснований[1], не отличающиеся существенно по геометрическим параметрам (Гуанин-Уридин и др). Кроме того, из Вобл-Гипотезы, да и просто из общей Криковской схемы (модели) кода, автоматически следует, что в кодонах (триплетах) генов только первые два нуклеотида (дублет) кодируют последовательности аминокислот в белковых цепях. Третьи же кодоновые нуклеотиды, не участвуют в кодировке аминокислотных последовательностей в белках. Эти третьи, хотя и детерминированы жестко молекулой ДНК, но допускают произвольные, случайные, не канонические спаривания с первыми нуклеотидами антикодонов транспортных РНК, переносящих аминокислоты. А посему эти первые нуклеотиды антикодонов могут быть любыми из 4-х возможных. Следовательно, третьи нуклеотиды в кодонах и спаривающиеся с ними первые в антикодонах, не имеют знакового характера и играют роль «стерических костылей», заполняющих «пустые место» в кодон-антикодоновых связках. Короче говоря, первый нуклеотид в антикодонах случаен, «воблирует» — от английского ‘wobble’ (качание, колебание, виляние). Вот суть Вобл-гипотезы. Если принять идею «стерических костылей», тогда ясно, что 3-й нуклеотид в омонимичных кодонах иРНК не участвует в кодировке аминокислот. На первый взгляд возникает некий генетико-семантический произвол и модель триплетного кода, вроде бы, теряет логику и очевидный смысл. Подтверждая это, приведем слова фактического автора теории триплетного кода, Френсиса Крика, начертанные им в своей автобиографической книге незадолго до смерти [Crick, 1989, стр. 98]: «Важно отметить, что структура генетического кода не имеет очевидного смысла, хотя определенные закономерности все же наблюдаются – в некоторых случаях это одни и те же первые два основания в кодонах, кодирующие одну аминокислоту, тогда как третье может быть любым». Уточним. 3-й нуклеотид в кодоне теоретически может быть любым из 4-х возможных, поскольку спаривается с 1-м антикодона случайно, и эта пара, как уже говорилось, не участвует в кодировке аминокислот. Но, еще раз, в реальности 3-и кодоновые нуклеотиды детерминированы исходной ДНК и ничего канонического не нарушают. Нарушают каноны именно 1-е антикодоновые, комплементарные 3-м кодоновым. Удивительно, Ф.Крик видел синонимическую вырожденность кода, но не видел омонимическую. Хотя его фраза «…код не имеет очевидного смысла» говорит нам, что гениальный мозг Ф.Крика сознавал ограничения предложенной им модели и неоднозначности, связанные с 1-м «воблирующим» антикодоновым нуклеотидом, когда иРНК покодонно читается рибосомой в комплексе с тРНК по правилу «два из трёх». И этот комплекс ‘рибосома-иРНК-тРНК’ неизбежно должен решать типично лингвистическую смысловую проблему омонимии. Иначе ошибки в синтезе белков неизбежны.«Два из трёх» как признак квази сознания генома
Поставим такой вопрос: «воблирование» — синоним случайности, но случайно ли «воблирование»? Представляется, что это псевдослучайность. Обоснуем фундаментальную важность явления «как бы» случайности 1-го нуклеотида в антикодонах в омонимичных ситуациях при синтезе белков рибосомой. Связка 3-й—-1-й нуклеотиды в кодон-антикодоне в омонимичной ситуации намеренно не является элементом знаковой структуры рибосомной техники «чтения» иРНК. Причина этого в том, что, кроме прочего, белковый код является ментальной структурой, работающей с текстами иРНК, текстами не в метафорическом смысле (поэтому кавычки убираем), а с реальными текстами-мыслями, текстами-командами. Обсуждаемая «как бы» случайность необходима. Она дает гибкость коду, позволяя биосистемам в ходе естественного отбора осуществлять «белковый поиск», синтезировать «пробные белки», приспосабливаясь к переменчивым в геологических масштабах условиям внешней среды. Вот почему эта случайность необходима. Белковый код синонимично щедр, богат, избыточен. Но одновременно он врастает через омонимию в другие — смысловые ареалы генетического кодирования на текстовом уровне иРНК, а возможно, и пре-иРНК.
Итак, мы имеем два вектора кода белков синонимический и омонимический. Первый обеспечивает избыточность информации по выбору аминокислот. Второй обеспечивает выход из неопределенных ситуаций при их выборе, базируясь на фундаментальном атрибуте генетической информации – её лингвистичности. Если бы организмы автоматически руководствовались моделью кода в канонических Криковских рамках, следовали бы ей без каких-либо поправок, то жизнь на Земле была бы невозможна. Однако в этом отношении все относительно спокойно. Синтез белка – достаточно точный процесс именно потому, что он использует приемы, свойственные лингвистике и логике. Рибосомный аппарат и геном в целом есть квази разумная система, читающая текст иРНК потриплетно (локально, по частям) и, вместе с тем, как целое: континуально, нелокально. Именно нелокальность чтения снимает проблему омонимии. Каким образом это происходит?
Еще раз обратимся к полузабытой и недооцененной статье Лагерквиста, но не для того, чтобы снова и снова критиковать триплетную модель белкового кода. Она сыграла свою, отнюдь не слабую, роль в развитии генетики и биологии в целом. Наша цель другая – понять белковый код как дуалистичную знаковую систему, оперирующую на основе слепой физико-химии, с одной стороны, и, одновременно, с использованием квази смысловых построений текстов ДНК и РНК и квази ментальных функций генома, с другой. Триплетный код – лишь одна из множества подсистем кодирования и создания динамичного образа будущего организма, причем низшая подсистема. Непонимание этого тормозит развитие биологической мысли, приводит к достаточно бессмысленным и дорогим программам исследований. Лагерквист, увидевший противоречивость триплетной модели белкового кода, но не понявший причины, пытался вывести модель кода из логического тупика, но безрезультатно. Он ничего не мог противопоставить очевидному и странному, что правило «два из трех» выполняется для рибосомной трансляционной машины также и в условиях in vivo, цитируем, «с частотой, которую нельзя не принять во внимание». Далее Лагерквист пишет: «если это так, клетка с определенной вероятностью могла бы читать неправильно, и это будет означать наличие угрозы неправильной трансляции, если метод «два из трех» был бы использован не подходящим образом. В любых кодоновых семействах это ведет к ошибкам в белковом синтезе». Однако что есть «использование не подходящим образом» правила «два из трех» для большинства генетиков остается вне поля зрения. Видимые логические противоречия модели попросту игнорируются, поскольку рибосомы de facto не ошибаются с выбором аминокислот. Отсюда соблазн считать триплетную модель корректной. Однако зияющие дыры в «канонической» модели кода становятся все шире и заметнее.
Чтобы выйти из омонимического тупика необходима простая, но ключевая идея: вновь обратиться к лингвистике и почерпнуть оттуда понятие контекста, которое снимает проблему омонимии. Омоним утрачивает неоднозначность только в контексте, т.е. роль части становится ясной, когда ее рассматривают в составе целого. И контекст (целостный текст) иРНК — отнюдь не метафора. Как-то исподволь, задним числом молекулярные биологи и генетики признают это, используя идею «второго генетического кода» [Овчинников Л.П., http://bio.fizteh.ru/student/files/biology/bioarticles/f_4ai2]. Цитируем Л.П.Овчинникова, одного из видных молекулярных биологов: «Инициирующий кодон узнается только в определенном контексте. Если мы зададим вопрос, можно ли, имея перед собой последовательность нуклеотидов какой-либо иРНК, таблицу генетического кода и зная, что трансляция иРНК идет в направлении от 5′- к 3′-концу, а белковая цепочка растет от N-конца к C-концу, написать последовательность аминокислот белка, закодированного в этой иРНК, то будем вынуждены ответить на поставленный вопрос отрицательно. … Нельзя определить, с какого места иРНК мы должны начать переводить последовательность нуклеотидов в последовательность аминокислот. Уже очень давно стало ясно, что начало трансляции иРНК не совпадает с началом самой иРНК. Свидетельством этому служат полицистронные иРНК бактерий, в которых инициация белкового синтеза происходит на каждом цистроне, а также присутствие в иРНК про- и эукариот 5′-концевых нетранслируемых последовательностей. Вместе с тем установлено, что биосинтез белка как у про-, так и у эукариот, всегда начинается с одной и той же аминокислоты — метионина. Можно было бы предположить, что трансляция информации, закодированной в иРНК, начинается с первого от 5′-конца метионинового кодона, которым является триплет AUG. Для многих моноцистронных эукариотических иРНК это действительно так, хотя бывают и исключения. Однако это совсем не так для полицистронных иРНК бактерий, где инициация часто происходит на триплетах AUG, отстоящих очень далеко от начала иРНК. Этим триплетам может предшествовать большое количество других AUG, на которых инициации не происходит. Более того, оказалось, что первый метионин в белке в некоторых случаях включается не на метиониновом кодоне AUG, а на кодоне GUG, который соответствует в таблице генетического кода аминокислоте валину. Иногда инициация с метионина может происходить и на других кодонах: AUA и AUU (кодонах изолейцина), UUG и, возможно, CUG (кодонах лейцина). Стало очевидным, что для узнавания кодона в качестве инициирующего важен не только сам и, может быть, не столько сам кодон, но какой-то контекст, делающий его инициирующим. У эукариот инициация происходит… чаще всего с первого AUG, однако только в том случае, если этот AUG находится в оптимальном контексте: за два нуклеотида до него обязательно должен находиться пурин (A или G), а непосредственно за ним должен следовать G. Если первый AUG в эукариотической иРНК находится не в оптимальном контексте, он пропускается и инициация начинается со следующего AUG. Для такой инициации очень важно также наличие кэп-структуры на 5′-конце иРНК и, как ни странно, поли(А) последовательности на противоположном конце молекулы. Кэп-структура и поли(А) последовательность узнаются специфическими белками, которые также необходимы для инициации. При таком способе инициации трансляции у эукариот последовательность иРНК как бы просматривается (сканируется) с начала иРНК (от ее кэп-структуры) для поиска кодона AUG в оптимальном контексте. Такая инициация получила название «кэп-зависимая инициация по сканирующему механизму. Сравнительно недавно было показано, что аминокислота селеноцистеин (очень редкая, но функционально очень важная аминокислота) непосредственно включается в белок. Возникает закономерный вопрос, как же закодирована эта аминокислота. Ведь значение всех 64 возможных кодонов уже четко определено, и все они используются в кодировании двадцати стандартных аминокислот и сигналов терминации. Исследования показали, что селеноцистеин кодируется UGA (терминирующим кодоном в таблице генетического кода), если за ним находится особая стимулирующая последовательность. Эта последовательность может отстоять от UGA на очень большом расстоянии — иногда она может быть на расстоянии 200 нуклеотидов и находиться в 3′-нетранслируемой области иРНК».
Как видим из этой длинной, но чрезвычайно важной цитаты, классическая молекулярная биология, а вслед за ней генетика, вынуждены занять идею контекста у лингвистики (но только в метафорическом смысле). И второе, не менее важное, положение также вводится – это фактор дальнего влияния определенных иРНК-блоков (кэп, поли(А), стимулирующие посследовательности) на далеко удаленное в иРНК место включение рибосомой первой определенной аминокислоты в синтезирующуюся белковую цепь. Понадобилась и дополнительная идея «просмотра-сканирования» всей иРНК, т.е. контекста иРНК. Все эти объясняющие факторы в общем виде предсказаны нами ранее. В том числе и механизм сканирования полинуклеотидов за счет солитонных возбуждений РНК и ДНК (Гаряев, 1997). Заметим также и другой важный момент – перекодировки кодонов в зависимости от контекстов, что также никак не укладывается в прокрустово ложе канонической триплетной модели.
Процитируем и дальше Л.П.Овчинникова. «Некоторые иРНК содержат сигналы на изменение рамки считывания. Некоторые иРНК содержат в транслируемой области терминирующие кодоны, но эти кодоны успешно обходятся за счет изменения рамки считывания перед ними или непосредственно на них. Рамка может сдвигаться на -1, +1 и + 2. Существуют специальные сигналы в иРНК, изменяющие рамку считывания. Так, сдвиг рамки трансляции на -1 на РНК ретровируса происходит на специфической гептануклеотидной последовательности перед шпилечной структурой в иРНК. Для сдвига рамки на +1 на иРНК бактериального фактора терминацинации RF-2 важны нуклеотидная последовательность на месте сдвига (кодон UGA), последующий кодон, а также предшествующая им последовательность, комплементарная к 3′-концевой последовательности рибосомной РНК (аналог последовательности Шайна-Дальгарно)».
Ясно, что такие сдвиги рамок считывания иРНК чистой физико-химией не объяснить, равно как и контекстные дальние влияния и «переосмысления» кодонов. Это уже иные знаковые измерения генома, переход на его логические операции как квантового компьютера [Gariaev, Birshtein et al., 2001].
«Считывание иРНК в пределах одного цистрона не всегда является непрерывным. Первоначально считалось, что последовательность нуклеотидов в иРНК всегда читается непрерывно от инициирующего до терминирующего кодона. Однако оказалось, что при трансляции иРНК гена 60 фага Т4 последовательность значительной длины может пропускаться. При этом рибосома совершает как бы прыжок по иРНК с одного глицинового кодона GGA, находящегося перед терминирующим кодоном UAG, на другой глициновый кодон GGA, который отстоит от первого на 50 нуклеотидов. Механизм этого явления пока не очень ясен».
Вот еще один из многочисленных примеров, когда официальная наука пасует перед фактом, не укладывающемся в каноны и догмы. Действительно, такие «как бы прыжки» рибосомы должны быть результатом реального прочтения и понимания смысла иРНК. И здесь уже нет места аллегории или метафоре. Все эти отклонения от канонов триплетной модели и называют сейчас «вторым генетическим кодом». Что это за код? Какие механизмы лежат в его основе? Надо полагать, что ключевой из них – лингвистические потенции молекул ДНК и РНК, которые являются, по сути, реальными ментальными конструкциями. Только в этом, не метафорическом варианте, мы можем понять истинный смысл перечисленных примеров отступления от якобы «общих» правил трансляции генетической информации с текстов иРНК. Подведем промежуточный итог фундаментальных явлений, которые официальная наука вынуждена констатировать, причем, без объяснений (их у нее нет):
а) дистантность контекстного влияния удаленных иРНК последовательностей на точное осмысление кодона, читаемого рибосомой, и на его перекодировки,
б) нелокальное сканирование больших протяженностей иРНК,
в) смысловые сдвиги рамок считывания иРНК,
г) дальние «прыжки» рибосом по иРНК,
д) перекодировки кодонов.
Попытаемся понять, что происходит в контекстных ситуациях, включая омонимические с кодирующими дублетами (правило Лагерквиста «два из трех»). Принявши тезис о квази разумности генома, мы обязаны трактовать генетические омонимии точно также как это делается в лингвистике. А именно: информационная нагрузка омонима открывается только при прочтении и понимании текста как целого (или достаточно большой части его), т.е. контекста, независимо от того, человеческий это текст или генетический. Мы не можем понять смысл омонима ‘лук’ и омонима ‘коса’ вне целой фразы или предложения. Аналогично рибосомная трансляционная «машина» должна прочитать и понять весь текст иРНК, или большую его часть, чтобы на этом основании принять точное решение о выборе одного из двух омонимических (одинаковых) дублетов кодонов, кодирующих разные аминокислоты и/или стоп-сигналы. Или принять решение о «прыжке» рибосомы на определенное расстояние. То же относится к ситуациям перекодировок кодонов, но здесь, вероятно, понятие контекста имеет более широкий ареал, уходящий за рамки лингвистики. Например, в случае аминокислотного голодания или при тепловом шоке. В этом случае биосистемой, как «контекстные» учитываются критические ситуации эколого-биохимического характера, требующие сиюминутных или длительно эволюционных адаптаций с последующей закачкой новых аминокислот и синтеза новых пробных белков. Вообще, отношение к синтезу белков должен существенно измениться. Этот процесс нельзя более воспринимать как чисто физико-химические акты взаимодействий ДНК, РНК, ферментов, белков рибосом, аминокислот и других метаболитов. Здесь мы имеем один из бесчисленных примеров разномасштабной разумности, как всего организма, так и тканей, клеток и генома в целом.Исторически сложилось, что лингвистическая терминология по отношению к белковому коду используется давно и повсеместно. А именно с момента, когда в начале 60-х годов прошлого века Ф.Крик и М.Ниренберг молекулу ДНК стали называть текстом. Это было гениальное предвосхищение, но Ф.Крик и большинство, использующих такой прием и поныне, понимают текстовость ДНК, РНК и белков как метафору, беря взаймы у лингвистики ее ментальное начало. Пусть «классические генетики» допустят на минуту, что эти термины по отношению к хромосомному аппарату — не метафоры. Тогда логично принять сильное положение, что белоксинтезирующая система и геном обладают малой частью сознания и мышления или их аналогом форме биокомпьютинга [Гаряев и др., 1997; Gariaev, Birshtein et al., 2001]. Природа объединяет разумным началом реальные физико-химические и квантовые акты в архисложной метаболической сети белкового синтеза. Хотя идея геномного компьютинга in vivo это также всего лишь модель, но модель, существенно более развитая по сравнению с пониманием белкового биосинтеза как чистой физикохимии и биохимии. Геном по своему разумен. Такое восприятие восходит к Аристотелю, к его постулату энтелехии, а далее к Дришу. К этому повороту, а точнее, возврату на новом уровне к формуле ‘causa finale’, официальная генетика не готова до сих пор. Она тормозит мысль биологов в этом направлении, что контрпродуктивно. Это застой, и мы видим следствия – традиционная генетика, и вслед за ней медицина, не могут и не смогут решить ни проблему рака, ни проблему туберкулеза, СПИДа, продления жизни людей и т.д. Но выход есть. Это переход к принятию иных, биосемиотических, конструкций генома, о чем здесь и идет речь. Тут уже многое сделано. Биосемиотический аспект генетики блестяще представлен в работах Седова и Чебанова, а также несколькими зарубежными исследователями [http://www.zanoza.lv/blog/gordon/430]. Они видят в геноме не только текстовость, но и эстетические направляющие: «Во многих участках ДНК выявлены рефрены — «темы с вариациями», ритмические и смысловые повторы, напоминающие омонимы, поэтические рифмы и музыкальные темы». Отдельно о ДНК-белковых музыкальных темах. На Западе производство и торговля ДНК- и Белковой ‘музыкой’ поставлено на поток. Нуклеотиды и аминокислоты в ДНК и белковых последовательностях по определенным алгоритмам переобозначаются нотами. Получаются отнюдь не хаотические звуки, но фактически музыка. Ее даже пытаются использовать как лечебный фактор. Любая поисковая система в Интернете выдаст массу ссылок на словосочетание ‘DNAmusic’ или ‘Proteinmusic’. Иными словами, игнорируя генетический официоз, дельцы безоглядно и безответственно эксплуатируют зачаточное понимание волновых, в том числе музыкальных, знаковых функций генетических структур. Думается, что это достаточно опасно, поскольку прослушивание такой музыки, неконтролируемо и без знания последствий, вводит в наш метаболический «ДНК-Белковый котел» волновые информационные вектора мало изученного действия.
Приведем еще один пример, демонстрирующий определенную разумность генома, причем в области, которая считается полигоном чистой случайности – в естественном мутационном процессе, где, как полагают, царит хаос, стохастика. Хотя, надо подчеркнуть, что понятие хаоса, как абсолютной неупорядоченности, ушло в прошлое. Прежде, до открытия ДНК, этот хаотический мутационный
 Предыдущий пост
Предыдущий пост

